Kampf gegen multiresistente Keime
07.02.2020Viele bakterielle Krankheitserreger entwickeln Resistenzen gegen Antibiotika. Bei der Suche nach neuen Therapiestrategien setzen Würzburger Forschungsgruppen auch auf digitale Technologien. Dafür gibt es Millionen vom Freistaat.
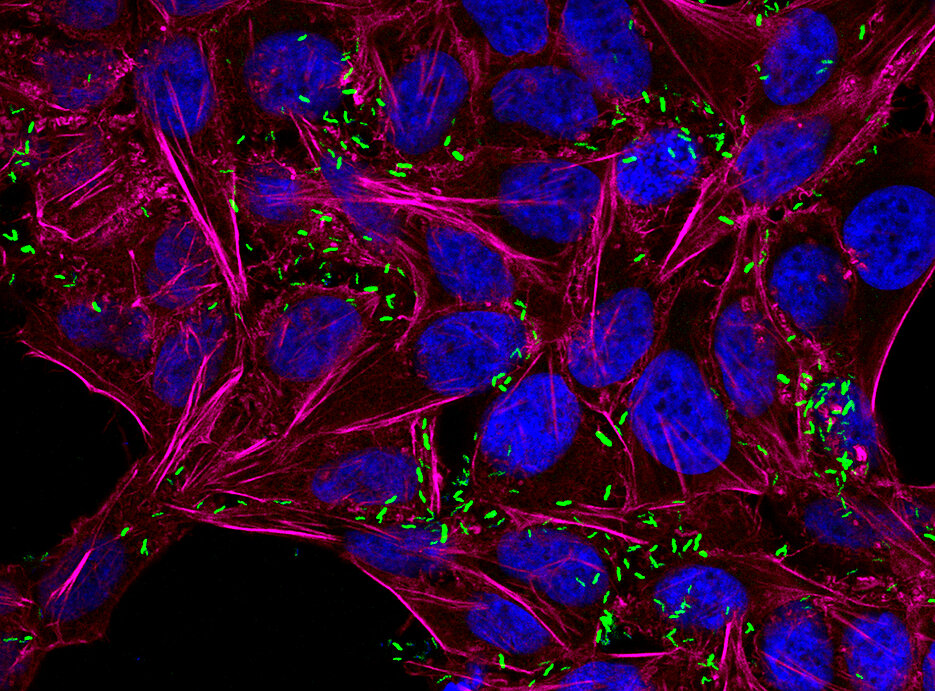
Grundlegend neue Ansätze gegen multiresistente Keime entwickeln: Das ist das Ziel des neuen bayerischen Forschungsnetzwerks bayresq.net. Der Freistaat stellt dafür über zehn Millionen Euro zur Verfügung. Forschungsgruppen der Julius-Maximilians-Universität (JMU) Würzburg sind an zwei der sechs geförderten Projekte beteiligt. Sie erhalten in den kommenden fünf Jahren rund 2,7 Millionen Euro.
Mit digitalen Methoden zu RNA-Antibiotika
Herkömmliche Antibiotika wirken üblicherweise gegen ein breites Spektrum von Bakterien. So wirkungsvoll sie sein mögen, fördern sie leider auch die Entwicklung multiresistenter Keime. Außerdem zerstören sie die schützende Mikrobiota – dazu gehören zum Beispiel Bakterien, die im Darm des Menschen nützliche Effekte ausüben.
Mit einem interdisziplinären Ansatz will ein JMU-Team um Professor Jörg Vogel, Juniorprofessor Lars Barquist und Nachwuchsgruppenleiterin Dr. Franziska Faber neue Antibiotika erforschen, mit denen sich gezielt einzelne Bakterienarten behandeln lassen. Prinzipiell können solche neuartigen Antibiotika auf Basis der Nukleinsäure RNA nach einfachen chemischen Prinzipien „programmiert“ und beim Auftreten von Resistenzen auch wieder umprogrammiert werden.
„Die Digitalisierung ist längst in den Lebenswissenschaften angekommen und das Problem der Antibiotikaresistenz muss aus verschiedenen Blickwinkeln betrachtet werden“, sagt Jörg Vogel. „Die Förderung durch bayresq.net wird es uns erlauben, digitale Strategien, die Hand in Hand mit unserer Arbeit im Labor gehen, zur Bekämpfung multiresistenter Keime zu entwickeln.“
Ziel des Projekts am Institut für Molekulare Infektionsbiologie / Zentrum für Infektionsforschung (IMIB / ZINF) der JMU ist es, universale Regeln zur Programmierung wirksamer Antibiotika zu entwickeln und die zu Grunde liegenden Mechanismen zu entschlüsseln. Dazu setzt das Team unter anderem eine Kombination aus Hochdurchsatz-Sequenzierung und maschinellem Lernen ein. Damit soll eine sehr leistungsfähige, digitale Plattform für die zukünftige Anwendung RNA-basierter Antibiotika gegen eine Vielzahl von Bakterien geschaffen werden.
Salmonellen und Campylobacter im Stresstest
Krankheitserreger sind während des Infektionsprozesses vielen unterschiedlichen chemischen Reizen und Stressbedingungen ausgesetzt. Diese Reize gehen vom Wirtsorganismus, der Mikrobiota und der Nahrung sowie von Antibiotika und anderen Medikamenten aus.
Um sich diesen wechselnden Bedingungen anzupassen oder sie zu umgehen, besitzen Krankheitserreger diverse Überlebens- und Anpassungsstrategien. Hier ist aber noch weitgehend unklar, welche Stressantworten auf bestimmte Reize folgen und welche molekularen Mechanismen dem zu Grunde liegen.
Hier setzt das StressRegNet-Konsortium an, das von Professorin Cynthia Sharma vom IMIB / ZINF und von Nachwuchsgruppenleiterin Dr. Ana Rita Brochado vom ZINF / Biozentrum gemeinsam mit Professor Christian Müller vom Institut für Statistik der Ludwig-Maximilians-Universität München geleitet wird.
Das Team will unterschiedliche chemische Reize und regulatorische Signalwege untersuchen, welche die Wirtsanpassung von Salmonellen und Campylobacter steuern. Beides sind weitverbreitete Lebensmittelkeime, die vor kurzem von der Weltgesundheitsorganisation WHO mit hoher Priorität für die Erforschung und Entwicklung neuer Antibiotika eingestuft wurden.
Mittels Hochdurchsatz-Automationstechnologien basierend auf einer Roboterplattform wollen die Forscherinnen und Forscher die beiden bakteriellen Krankheitserreger mehr als 3.000 unterschiedlichen Signalmolekülen aussetzen. Dann werden die hiervon ausgelösten Genexpressionsantworten und Stressreaktionen gemessen, wobei der Fokus auf der Regulation durch kleine RNA-Moleküle liegt.
Die Messungen werden einen hoch komplexen Datensatz liefern. Dieser wird anschließend mit maschinellen Lernverfahren auf bestimmte Signale und Stressantworten im Zusammenhang mit Antibiotika-Sensitivität und Wirtsinteraktionen untersucht.
Das StressRegNet-Konsortium möchte damit einen bedeutenden Fortschritt im Hinblick auf die Automatisierung und Digitalisierung in der Infektionsbiologie erreichen. Seine Arbeit soll zugleich wertvolle neue Einblicke in die regulatorischen Netzwerke der Bakterien liefern. Für die Entwicklung neuer antimikrobieller Strategien ist dies von essentieller Bedeutung.
Fakten zum Forschungsnetzwerk bayresq.net
Die sechs Projekte des Netzwerks „Neue Strategien gegen multiresistente Krankheitserreger mittels digitaler Vernetzung – bayresq.net“ laufen an der JMU, der Universität Erlangen-Nürnberg, der LMU, der Technischen Universität München und an der Universität Regensburg. Eingebunden sind Forschungsgruppen aus Biologie, Bioinformatik, Chemie, Biophysik, Medizin und Mathematik.
In den Würzburger Projekten sind neben Juniorprofessor Lars Barquist von der JMU/HIRI zwei Nachwuchsgruppenleiterinnen des ZINF vertreten. Dr. Franziska Faber forscht seit 2018 am ZINF; Dr. Ana Rita Brochado wurde 2019 als Nachwuchsgruppenleiterin an das ZINF / Biozentrum (Lehrstuhl für Mikrobiologie, Professor Thomas Rudel) berufen. Sie wird zudem über das Emmy-Noether-Programm der Deutschen Forschungsgemeinschaft (DFG) gefördert.
ZINF: Nachwuchsgruppen als Herzstück
Das Zentrum für Infektionsforschung (ZINF) der JMU wurde 1993 gegründet und ist die älteste universitäre Einrichtung Deutschlands, die sich interdisziplinär und fakultätsübergreifend der Erforschung von Infektionskrankheiten widmet. Seit 2010 ist es eine zentrale wissenschaftliche Einrichtung der JMU.
Herzstück des ZINF sind die Nachwuchsgruppen, die jungen, talentierten Forschenden nach ihrer Postdoc-Zeit die Möglichkeit geben, ihr eigenes Labor aufzubauen. Die ZINF-Nachwuchsgruppen haben sich in den vergangenen 25 Jahren zu einem international renommierten Programm entwickelt. Dessen Erfolg lässt sich auch daran ablesen, dass viele ehemalige Nachwuchsgruppenleiter im Anschluss an ihre Zeit am ZINF auf nationale und internationale Professuren oder unbefristete Gruppenleiterstellen berufen wurden.
„Durch das ZINF-Nachwuchsgruppenprogramm konnte in den letzten Jahren immer wieder neue Expertise in hochaktuellen Technologien oder Forschungszweigen im Bereich der Infektionsforschung nach Würzburg rekrutiert werden. Beispielsweise ist die Expertise von Dr. Brochado im Bereich von genomweiten Screens mittels Hochdurchsatz-Automationstechnologien für unser StressRegNet-Konsortium essentiell“, sagt Cynthia Sharma.
Weblink
Bayerisches Forschungsnetzwerk bayresq.net
Kontakt
Prof. Dr. Jörg Vogel, Direktor des Instituts für Molekulare Infektionsbiologie, T +49 931 31-82575, joerg.vogel@uni-wuerzburg.de
Prof. Dr. Cynthia Sharma, Sprecherin des Zentrums für Infektionsforschung, +49 931 31-82560, cynthia.sharma@uni-wuerzburg.de