Am Uniklinikum Würzburg mitentwickeltes Anti-Leukämiemedikament in den USA zur Behandlung bei minimaler Resterkrankung zugelassen
04/11/2018Ende März dieses Jahres erteilte die US-amerikanische Food and Drug Administration in einem beschleunigten Verfahren die Zulassung des Immuntherapeutikums Blinatumomab für die Behandlung von Patienten mit minimaler Resterkrankung bei Akuter lymphatischer Leukämie. Das Medikament wurde am Uniklinikum Würzburg maßgeblich mitentwickelt.
Ende Januar dieses Jahres erschien in der Fachzeitschrift Blood der US-amerikanischen Gesellschaft für Hämatologie die Publikation zu einer von den Uniklinika Frankfurt und Würzburg aus geleiteten europa-weiten Studie, bei der Patienten mit einer minimalen Resterkrankung von Akuter Lymphatischer Leukämie erfolgreich mit dem Antikörper-Medikament Blinatumomab behandelt wurden. Das Uniklinikum Würzburg (UKW) berichtete hierrüber in einer Presseinformation am 8. Februar 2018. Jetzt, am 29. März dieses Jahres, gab die US-amerikanische Zulassungsbehörde Food and Drug Administration (FDA) nach einem beschleunigten Verfahren grünes Licht für einen generellen Einsatz des Immuntherapeutikums bei dieser Indikation. Für anders gelagerte Indikationen bestanden schon vorher Marktzulassungen von Blinatumomab – sowohl in den USA, wie auch in der EU.
Die Akute Lymphatische Leukämie (ALL) ist eine Form von bösartigem Blutkrebs. Bei 40 bis 50 Prozent der mit Chemotherapeutika behandelten Patienten bleibt mindestens eine minimale Resterkrankung (Minimal Residual Disease – MRD) bestehen. Patienten mit MRD-positiver Erkrankung erleiden praktisch immer ein klinisches Rezidiv. Durch die jetzt regulär mögliche Gabe von Blinatumomab lässt sich die Überlebenswahrscheinlichkeit dieser Hochrisiko-Gruppe in den USA deutlich verbessern.
In Deutschland steht Blinatumomab zur Zeit für die MRD-positive ALL nur im Rahmen klinischer Studien zur Verfügung. Mit einer regulären Zulassung durch die europäische Zulassungsbehörde für die EU wird im Lauf dieses Jahres gerechnet.
An der Erfindung, Entwicklung und klinischen Erprobung von Blinatumomab entscheidend beteiligt waren Prof. Dr. Ralf Bargou, der Direktor des am UKW angesiedelten Comprehensive Cancer Centers (CCC) Mainfranken, Dr. Marie-Elisabeth Goebeler, die Leiterin der Early Clinical Trial Unit am UKW, sowie Prof. Dr. Max Topp, der Leiter des Bereichs Hämatologie an der Medizinischen Klinik II des Würzburger Uniklinikums.
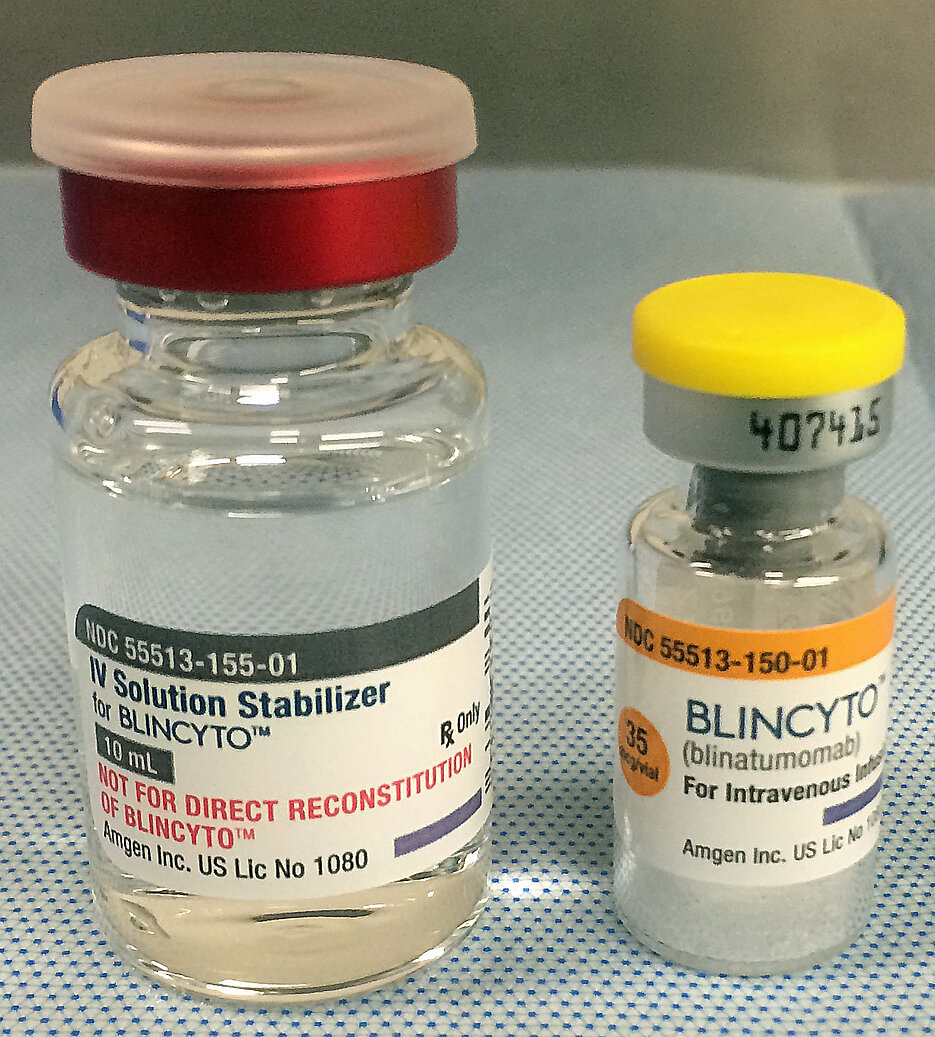
Über den Wirkstoff Blinatumomab
Blinatumomab gehört zu einer neuen Klasse von so genannten bispezifischen Antikörpern, die direkt das menschliche Immunsystem gegen Tumorzellen wirken lassen. Es spannt die körpereigenen T-Zellen, eine Form der Lymphozyten, ein, um Leukämiezellen zu vernichten. Diese „Killer“ können in der Regel Krebszellen nicht von gesunden Zellen unterscheiden und greifen sie deshalb auch nicht an. Den Forschern gelang es, diese biochemische Blindheit zu überwinden, indem sie gentechnisch einen Antikörper designten, der einerseits in der Lage ist, an der Krebszelle anzudocken und andererseits an T-Zellen binden kann. Mit Hilfe dieses „Adapters“ werden die Abwehrzellen aktiviert, sie erkennen die schädlichen Zellen und können sie in der Folge zerstören.