Arbeitsgruppe Gohla
Zielgerichtete pharmakologische Strategien zur Behandlung von Krebs
Zur Behandlung von Krebs werden Medikamente eingesetzt, die das Tumorwachstum durch Schädigung der DNA oder der Zellteilung hemmen, und so zum Zelltod führen. Allerdings werden mit diesen Wirkstoffen auch gesunde Zellen und Gewebe getroffen, wodurch es zu schweren unerwünschten Wirkungen kommen kann.
Bei Krebserkrankungen können genetische und epigenetische Veränderungen zu einem veränderten Tumor-Stoffwechsel führen, und entscheidend zur Pathologie und zur Resistenzentwicklung gegen Medikamente beitragen. Es besteht daher ein großes Interesse an Wirkstoffen, die möglichst selektiv in den Tumor-Stoffwechsel eingreifen. Versuche, solche Medikamente zu entwickeln, fokussieren bisher auf Haupt-Stoffwechselwege der zellulären Energiegewinnung und der Produktion molekularer Bausteine zur Zellvermehrung. Allerdings sind diese Prozesse auch für viele gesunde Zellen lebenswichtig.
Parallel zu den bereits gut bekannten Ab-, Um-, und Aufbauwegen zellulärer Brenn- und Baustoffe laufen ‚im Untergrund‘ jedoch auch erst kürzlich entdeckte metabolische Reparaturprozesse ab, die für einen kontinuierlichen Stoffumsatz nötig sind. Unser Ansatz zielt auf den gesteigerten Bedarf an Reparaturprozessen im hochaktiven Metabolismus krankheitsassoziierter Zellen ab. Durch die pharmakologische Blockade wichtiger Stoffwechsel-Reparaturprozesse soll zum Beispiel erreicht werden, dass sich Tumorzellen oder fehlgesteuerte Immunzellen abhängig von ihrer Stoffwechselaktivität durch das Anhäufen toxischer Nebenprodukte selbst unschädlich machen.
Die pharmakologische Beeinflussung metabolischer Reparaturenzyme ist auch bei kardiometabolischen Krankheiten und Erkrankungen des zentralen Nervensystems von Interesse.
Unser Schwerpunkt liegt auf der Identifizierung und mechanistischen Charakterisierung geeigneter pharmakologischer Zielstrukturen, und der Entwicklung experimenteller Wirkstoffe.
Wir verwenden interdisziplinäre Ansätze, die von der Biochemie über die Molekular- und Zellbiologie bis hin zu Krankheitsmodellen reichen. Außerdem arbeiten wir eng mit Experten für Strukturbiologie, Hochdurchsatz-Screening Verfahren, medizinischer Chemie und Metabolomik, sowie mit klinischen Partnern zusammen.
Die Phosphoglykolat Phosphatase PGP (auch AUM genannt) ist ein prototypisches Stoffwechselreparatur-Enzym im Glukose-Metabolismus, das seit einigen Jahren im Fokus unseres Interesses steht.
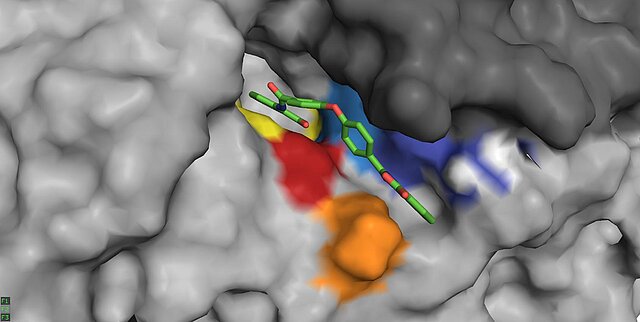
Vor Kurzem konnten wir zeigen, dass PGP ein pharmakologisch nutzbarer Angriffspunkt ist. Wir konnten erstmals einen Wirkstoff identifizieren, der zielgerichtet die PGP-Aktivität hemmt, und die Proliferation von Krebszellen blockiert (Jeanclos et al., 2022).
In weiterführenden Arbeiten sollen PGP-Inhibitoren der nächsten Generation entwickelt und in Krankheitsmodellen validiert werden.
Ausgewählte eigene Arbeiten zu PGP:
Jeanclos E, Schlötzer J, Hadamek K, Yuan-Chen N, Al-Wahsh M, Hollmann R, Fratz S, Yesilyurt-Gerhards D, Frankenbach T, Engelmann D, Keller A, Kaestner A, Schmitz W, Neuenschwander M, Sotriffer C, Hergenröder R, von Kries JP, Schindelin H, Gohla A. Glycolytic flux control by drugging phosphoglycolate phosphatase. Nature Communications, DOI:10.1038/s41467-022-34228-2
Segerer G, Engelmann D, Kaestner A, Trötzmüller M, Köfeler H, Stigloher C, Thiele C, Jeanclos E, Gohla A (2018). A phosphoglycolate phosphatase/AUM-dependent link between triacylglycerol turnover and epidermal growth factor signaling. Biochim Biophys Acta – Mol Cell Biol Lipids 1863, 584-594
Segerer G, Hadamek K, Zundler M , Fekete A, Seifried A , Mueller MJ , Koentgen F, Gessler M, Jeanclos E, Gohla A (2016). An essential developmental function for murine phosphoglycolate phosphatase in safeguarding cell proliferation. Sci Rep 6, 35160. doi: 10.1038/srep35160
Seifried A, Bergeron A, Boivin B, Gohla A (2016). Reversible oxidation controls the activity and oligomeric state of the mammalian phosphoglycolate phosphatase AUM. Free Radic Biol Med 97, 75-84
Übersichtsarbeiten zu metabolischen Phosphatasen:
Seifried A, Schultz J, Gohla A (2013). Human HAD phosphatases: structure, mechanism, and roles in health and disease. FEBS J 280, 549-71
Gohla A (2019). Do metabolic HAD phosphatases moonlight as protein phosphatases? Biochim Biophys Acta – Mol Cell Res 1866, 153-166
Pyridoxal-5‘-Phosphat Phosphatase (PDXP/Chronophin) wurde ursprünglich von uns aus Hirngewebe gereinigt, massenspektrometrisch identifiziert, und funktionell charakterisiert (Gohla et al., 2005). PDXP hat primäre Funktionen im zellulären Vitamin B6-Metabolismus. Aktives Vitamin B6 (Pyridoxal-5‘-Phosphat/PLP) ist als Koenzym u.a. an der Biosynthese von Neurotransmittern beteiligt. PLP ist aber auch ein hochreaktives metabolisches Intermediat, das in freier Form toxisch wirken kann.
Wir konnten zeigen, dass die Abwesenheit von PDXP in Mäusen mit einem verringerten Wachstum von Hirntumoren (Schulze et al., 2016) und interessanterweise auch mit gesteigerten kognitiven Leistungen assoziiert ist (Jeanclos et al., 2019).
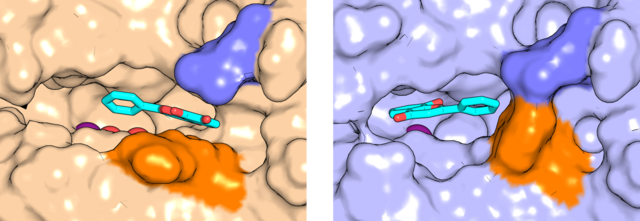
Neben dem Verständnis der zugrundeliegenden Mechanismen ist es ein weiteres Ziel unserer Arbeiten, PDXP-Inhibitoren zu entwickeln und in Krankheitsmodellen zu untersuchen. Kürzlich ist es uns gelungen, 7,8-Dihydroxyflavon als einen direkten PDXP-Inhibitor zu identifizieren (Brenner et al., 2024). Diese Substanz zeigt in verschiedenen ZNS-Erkrankungsmodellen häufig positive Effekte, obwohl ihr Wirkmechanismus noch unvollständig verstanden ist. Unsere neuen Erkenntnisse bieten eine Grundlage für die Entwicklung pharmakologischer PDXP-Inhibitoren zum Einsatz bei Störungen im ZNS oder bei Tumorerkrankungen.
Ausgewählte eigene Arbeiten zu PDXP:
Brenner M, Zink C, Witzinger L, Keller A, Hadamek K, Bothe S, Neuenschwander M, Villmann C, von Kries JP, Schindelin H, Jeanclos E, Gohla A (2024). 7,8-Dihydroxyflavone is a direct inhibitor of human and murine pyridoxal phosphatase. eLife, https://doi.org/10.7554/eLife.93094.3
Jeanclos E, Albersen M, Ramos RJJ, Raab A, Wilhelm C, Hommers L, Lesch KP, Verhoeven-Duif NM, Gohla A (2019). Improved cognition, mild anxiety-like behavior and decreased motor performance in pyridoxal phosphatase-deficient mice. Biochim Biophys Acta – Mol Basis Dis 1865, 193-205
Schulze M, Fedorchenko O, Sondergeld T, Knobbe-Thomsen C, Kraus S, Schwinn S, Beilhack A, Reifenberger G, Monoranu CM, Sirén AL, Jeanclos E, Gohla A (2016). Chronophin is a glial tumor modifier involved in the regulation of glioblastoma growth and invasiveness. Oncogene 35, 3163-77
Knobloch G, Jabari N, Stadlbauer S, Schindelin H, Köhn M, Gohla A (2015). Synthesis of hydrolysis-resistant pyridoxal 5'-phosphate analogs and their biochemical and X-ray crystallographic characterization with the pyridoxal phosphatase chronophin. Bioorg Med Chem 23, 2819-27
Kestler C, Knobloch G, Tessmer I, Jeanclos E, Schindelin H, Gohla A (2014). Chronophin dimerization is required for proper positioning of its substrate specificity loop. J Biol Chem 289, 3094-103
Gohla A, Birkenfeld J, Bokoch GM (2005). Chronophin, a novel HAD-type serine protein phosphatase, regulates cofilin-dependent actin dynamics. Nature Cell Biol 7, 21-9
Leberkrebs ist weltweit die vierthäufigste Ursache für krebsbedingte Todesfälle. Die Leberkrebs- Inzidenz und -Mortalität nimmt in der gesamten westlichen Welt weiterhin zu. Epidemiologische Daten deuten darauf hin, dass Adipositas und Fettlebererkrankungen eine wichtige Ursache für die kontinuierliche Zunahme hepatozellulärer Karzinome darstellen. Da diese Krebsarten besonders schwer mit derzeit verfügbaren systemischen Therapien zu behandeln sind, besteht ein dringender klinischer Bedarf an der Identifizierung effektiver therapeutischer Angriffspunkte.
In diesem Projekt soll die Rolle der Ferroptose an mit Fettleber-assoziierten hepatozellulären Karzinomen geklärt werden. Ferroptose ist eine Form des nicht-apoptotischen Zelltods, die durch die Eisen-abhängige Peroxidation von Phospholipiden charakterisiert ist. Peroxidierte Phospholipide entstehen fortlaufend im Stoffwechsel, und müssen durch verschiedene Lipid Reparatur-Enzyme entgiftet werden, um das Zellüberleben zu sichern. In Tumoren kann der Bedarf an diesen Entgiftungssystemen gesteigert sein. Unser Ziel ist es daher, Reparatursysteme für Lipid-Stoffwechselschäden zu identifizieren, die essentiell für das Überleben der Tumorzellen sind, und diese dann pharmakologisch zu inaktivieren. Als Testplattform für Wirkstoffe haben wir organotypische Leberschnittkulturen etabliert.